Суперинфекции 2: рубикон проблем, фиаско технологий и новая надежда
(c [1]) Phage therapy
Прошел 91 год со дня открытия пенициллина — первого препарата, совершившего революцию в эффективности лечения бактериальных заболеваний.
За почти век существования антибактериальных препаратов многие болезни практически забылись. Так, с 1947 г. считается, что Yersinia pestis, чумную бактерию, виновницу смерти 150 млн человек, удалось победить. И главным средством первого этапа лечения стали антибиотики.
Однако из-за роста вероятности возвращения забытых и появления новых инфекционных заболеваний Всемирная организация здравоохранения в последнее десятилетие бьет в набат. Причинами катастрофы стали халатность, глупость и эволюция. Скоро даже обычный порез на пальце может закончиться смертью. Но на подходе новые методы борьбы.
Первые проблемы
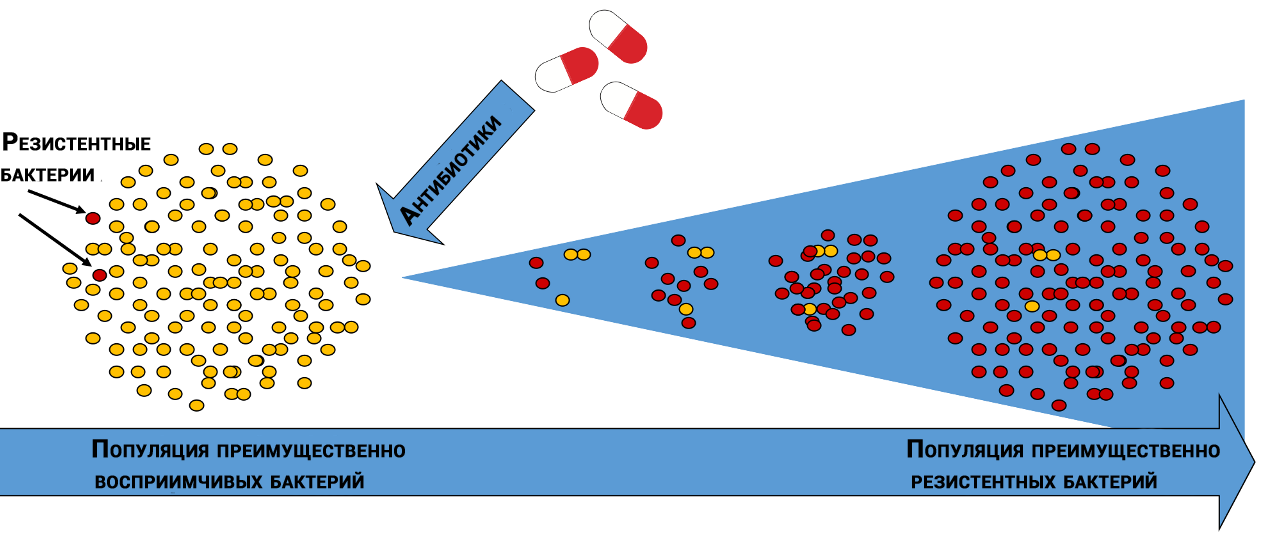
Естественный отбор антибиотикоустойчивых бактерий [2]
У разных популяций бактерий молекулы, на которые действуют антибиотики, имеют разную «чувствительность». Кроме того, бактерии одного и того же вида могут отличаться друг от друга, как снежинки — через многообразие жизнь всегда находит себе дорогу.
Случайным образом некоторые бактерии оказываются менее восприимчивы к действию антибиотика, и часть бактерий, уцелевшая после геноцида, даст потомство, которое вырастет и погибнет, но успеет оставить свое потомство, которое через ряд поколений создаст «идеальную» популяцию.
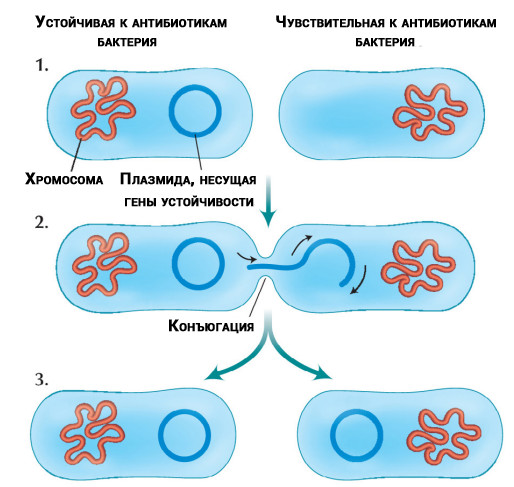
Перенос обособленных от хромосом молекул ДНК (плазмид), устойчивых к антибиотикам [3], между бактериями
Беда не приходит одна. Исследователи обнаружили [4], что некоторые бактерии могут передавать гены устойчивости другим бактериям как того же вида, так и другого. Перенос происходит независимо от того, присутствуют ли в лечении антибиотики или нет.
C момента открытия пенициллина чрезмерное использование антибиотиков существенно повлияло на развитие резистентности бактерий — невосприимчивости к антимикробным препаратам, что привело к появлению неизлечимых суперинфекций.
Перешагнуть Рубикон
Для снижения распространения резистентности к противомикробным препаратам в настоящее время используется инструмент AWaRe [5] (Access, Watch and Reserve), разработанный экспертами ВОЗ в виде списка [6] основных эффективных лекарственных средств.
В данном списке антибиотики разделяются на три группы: Access (доступность, препараты первого выбора), Watch (бдительность) и Reserve (резерв). Здесь определяется, какие антибиотики следует использовать лишь для конкретных бактерий, вызывающих наиболее распространенные заболевания, какие значительно увеличивают риск возникновения устойчивости, и какие необходимо применять в крайних случаях, при инфекциях с множественной устойчивостью.
На практике алгоритм действует следующим образом. В стерильный флакон набирают выделения из организма пациента (гной, раневое отделяемое, соскоб с бронха и т.д.) и отправляют в бактериологическую лабораторию, где определяют, какая именно бактерия находилась в материале, к каким антибиотикам она чувствительна, а к каким — устойчива.
Если бактерия не чувствительна к антибиотикам первой линии, врачи обращаются к менее используемым препаратам. Часть из них всегда должна быть в запасе и не применяться там, где могут справиться другие лекарства. Соответственно, и микроорганизмы меньше с ними знакомы и пока еще чувствительны.
По иронии судьбы среди антибиотиков резерва есть препараты, получаемые из самих бактерий. Например, колистин, произведенный в 1949 г., получен из бактерии Paenibacillus polymyxa. Этот антибиотик, как и другие из группы последнего резерва, применялся, как считалось, редко. Однако в 2015 г. нашлись резистентные к колистину бактерии.
Более 100 стран разработали национальные планы по борьбе с устойчивостью к противомикробным препаратам, но из них 75 % не имеют средств или мотивации для финансирования плана надлежащего применения антибиотиков.
В частности, Китай, невзирая на международные рекомендации, использовал [7] 12 тыс. тонн колистина (препарат резерва) в год для откорма свиней и предотвращения болезней у других животных.
При отсутствии ясного понимания, для чего необходим тотальный контроль распространения устойчивости к противомикробным препаратам, на помощь исследователям по всему миру приходит математика, которая позволяет моделировать различные ситуации и просчитывать риски развития резистентности, вплоть до фатальных. Наука с бессердечной точностью показывает, что грозит миру.
Фармацевтическое фиаско
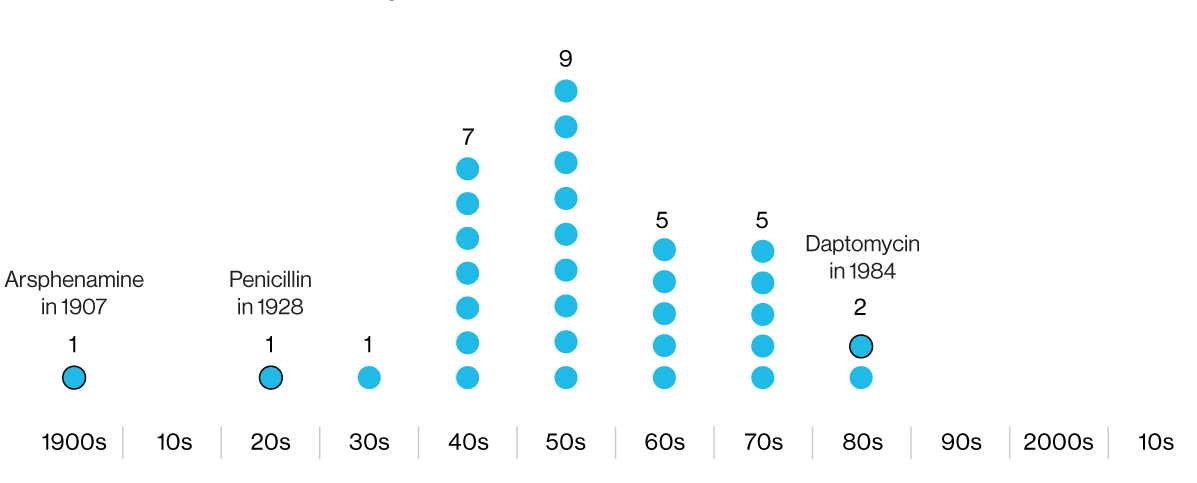
В инфографике указаны годы разработки антибиотиков, впоследствии веденных [8] в клиническую практику. Первый — арсфенамин — опасный мышьяксодержащий противомикробный химикат. Последний — даптомицин — утратил [9] эффективность против некоторых штаммов MRSA.
После пенициллиновой революции на полях сражений во время Второй мировой войны фармацевтическая промышленность вступила в «золотую эру» антибиотиков. Компании нанимали исследователей, миссионеров и путешественников со всего мира, чтобы собирать образцы почв в поисках новых антибактериальных соединений. Но «золотой век» стремительно сошел на нет, и в 1980-х годах настала «зима антибиотиков», которая продолжается до сих пор.
Сегодня разработка принципиально новых антибиотиков — редчайшее событие. Из полусотни препаратов, находящихся на разных стадиях клинических испытаний, менее дюжины [10] действительно инновационны.
Инвесторы руководствуются логикой, а не эмоциями: стоимость таких препаратов трудно повысить, так как общественность может возмутиться, и рассчитывать на регулярные поставки не стоит — по той причине, что препарат может попасть в резерв.
К тому же, потратив годы на поиск нового вещества и клинические исследования эффективности и безопасности, фармацевтические компании рискуют уже через месяцы после выхода на рынок «поймать» резистентность.
Из всех проверенных в двойных слепых плацебо контролируемых рандомизированных исследованиях за последние годы одобрили только восемь антибиотиков или их комбинаций: делафлоксацин, меропенем + ваборбактам, озеноксацин, плазомицин, эравациклин, имипенем + циластатин + релебактам, лефамулин.
Лефамулин, выпускаемый под брендом «Ксенлента», стал первым одобренным за 20 лет препаратом с новым механизмом действия против внебольничной бактериальной пневмонии. Показательно, что от безусловного медицинского триумфа производитель может ничего не получить.
Подобное уже случалось [11]. Так, компания Achaogen, потратив $250 млн, на протяжении 15 лет пыталась вывести на рынок новый антибиотик — плазомицин, после чего скоропостижно обанкротилась.
Учитывая актуальность проблемы, другие исследователи ищут новые прагматичные подходы в разработке методов сдерживания бактериального роста.
Всадники оптимизма

Стартап разработал платформу [12] для перепрограммирования бактерий на генетическом биопринтере, печатающем фрагменты ДНК длиной до 10 тыс. пар оснований.
Бостонская биотехнологическая компания Ginkgo Bioworks, поддержанная американским военным ведомством DARPA и венчурным фондом Y Combinator, вместо более эффективных антибиотиков создает [13] на биопринтере пробиотики — полезные бактерии, нацеленные на борьбу с «конкурирующими» резистентными микроорганизмами.
Не менее впечатляющий продукт разрабатывают [14] специалисты Locus Biosciences, взяв на вооружение метод редактирования генов CRISPR Cas3. Технология CRISPR известна благодаря использованию фермента Cas9, действующего как «генетические ножницы» для вырезания, редактирования и замены фрагментов ДНК.
Cas3 превосходит Cas9 широтой охвата — он способен влиять на длинные участки ДНК. CRISPR Cas3 целенаправленно воздействует [15] на бактерии и вирусы, и не просто режет, а эффективно стирает определенные последовательности ДНК — до 100 тыс. пар нуклеотидов за один раз.
В Locus Biosciences планируют использовать данную технологию для борьбы с опасными бактериями. В пользу метода играют большие размеры фермента Cas3 — он действует на бактериальные клетки, но слишком велик для проникновения в человеческую клетку и повреждения нашей ДНК.
Статью, наполненную смертью и разочарованием, хочется закончить на мажорной ноте. Мы не одиноки в борьбе с бактериями. Миллиарды лет вирусы-бактериофаги оставались одним из наиболее мощных инструментов контроля микробных популяций, но были почти не изучены на фоне успеха антибиотиков.
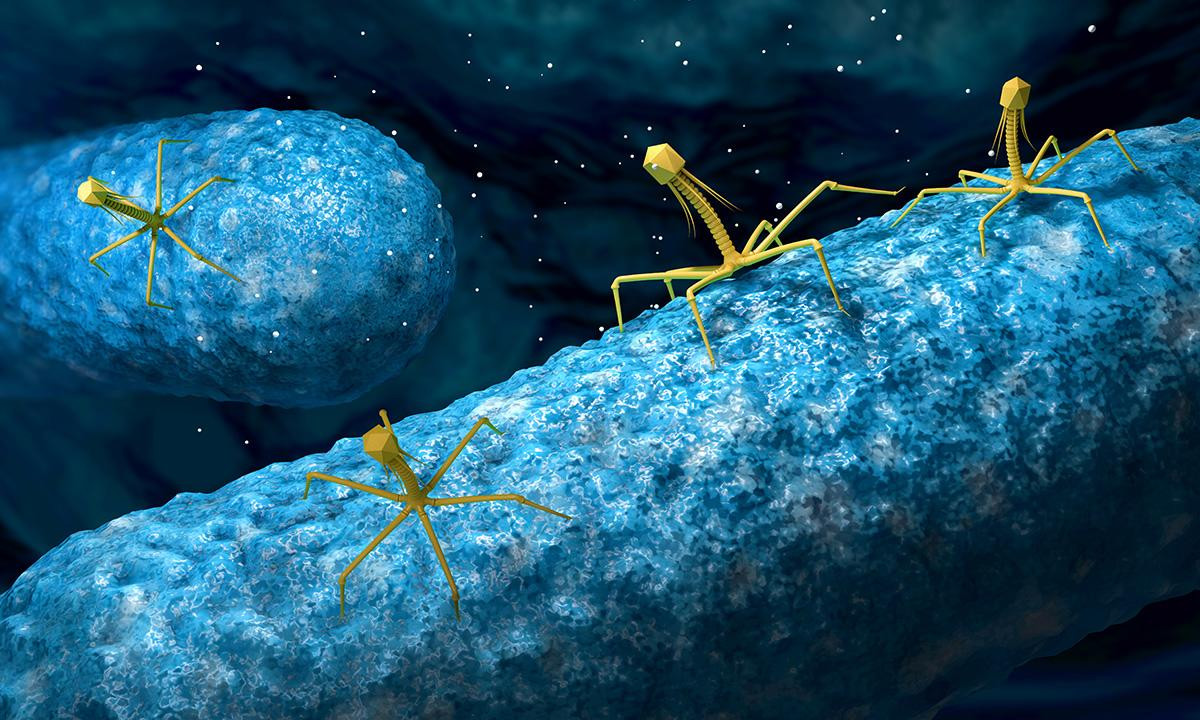
Фаги заняты любимым делом — атакуют бактерию [16].
После Второй мировой войны сложилась парадоксальная ситуация. В США и Западной Европе бактериофаги оставались в фокусе внимания только у биологов, а в странах Восточного блока из бактериофагов создавали реальные лекарства. В результате Россия стала мировым лидером по количеству зарегистрированных [17] бактериофаговых препаратов.
В США ренессанс бактериофагов случился только в последние годы. В мае 2019 г. были опубликованы результаты применения смеси трех типов бактериофагов на пациенте с трудноизлечимой инфекцией, вызванной одним из представителей нетуберкулезных микобактерий Mycobacterium abscessus. Результаты обнадеживают [18] — пациент пошел на поправку.
Уже начались исследования [19] ряда других природных и генетически модифицированных штаммов бактериофагов, но доступные массовому потребителю препараты, эффективные против некоторых бактерий, появятся только через несколько лет.
Несмотря на достижения, мы стоим в самом начале долгой и изнурительной борьбы с бактериями — главная битва впереди. Пока же большинство фагов не описаны [20] либо недоступны для генетических манипуляций.
Другие инструменты решения антибактериальной проблемы также далеко несовершенны. Тем временем без наращивания темпов химико-фармацевтических исследований нас ждут непростые десятилетия глобальных угроз.
В сентябре 2019 г. Глобальный комитет по мониторингу готовности (GPMB) [21] представил отчет «Мир под угрозой [22]», в котором признал реальной вероятность появления патогена, способного уничтожить в новой пандемии 50—80 млн человек.
Автор: randall
Источник [23]
Сайт-источник PVSM.RU: https://www.pvsm.ru
Путь до страницы источника: https://www.pvsm.ru/virusy/333428
Ссылки в тексте:
[1] c: https://www.vox.com/future-perfect/2019/5/14/18618618/phage-therapy-antibiotic-resistance
[2] Естественный отбор антибиотикоустойчивых бактерий: https://www.reactgroup.org/toolbox/understand/antibiotic-resistance/mutation-and-selection/
[3] устойчивых к антибиотикам: https://www.cddep.org/wp-content/uploads/2017/06/india_abx_report-2.pdf
[4] обнаружили: https://www.nature.com/articles/s41586-019-1521-8.epdf
[5] AWaRe: https://aware.essentialmeds.org/groups
[6] списка: https://aware.essentialmeds.org/list
[7] использовал: https://www.nature.com/news/spread-of-antibiotic-resistance-gene-does-not-spell-bacterial-apocalypse-yet-1.19037
[8] веденных: https://www.forbes.ru/tehnologii/352993-borba-za-vyzhivanie-pogibnet-li-chelovechestvo-iz-za-ustoychivosti-k-antibiotikam
[9] утратил: https://naked-science.ru/article/sci/stafilokokki-nauchilis-obmanyvat
[10] менее дюжины: https://www.who.int/medicines/areas/rational_use/antibacterial_agents_clinical_development/en/
[11] случалось: https://www.biopharmadive.com/news/achaogen-files-for-bankruptcy-protection-seeks-asset-sale/552737/
[12] платформу: https://xconomy.com/boston/2019/09/19/high-flying-ginkgo-nets-another-290m-to-program-cells-like-computers/
[13] создает: https://techcrunch.com/2014/07/16/why-the-first-yc-backed-biotech-company-may-just-be-the-future-of-pharma/
[14] разрабатывают: https://techcrunch.com/2016/12/21/move-over-cas9-crispr-cas3-might-hold-the-key-to-solving-the-antibiotics-crisis/
[15] воздействует: https://www.sciencedaily.com/releases/2019/04/190411172519.htm
[16] атакуют бактерию: https://cns.utexas.edu/news/explaining-the-science-a-look-at-the-potential-of-bacteriophages-in-a-post-antibiotics-world
[17] зарегистрированных: http://mosapteki.ru/material/lekarstvennye-sredstva-na-osnove-bakteriofagov-ch-2-6782
[18] обнадеживают: https://www.nature.com/articles/s41591-019-0437-z
[19] исследования: https://www.ncbi.nlm.nih.gov/pubmed/26795692
[20] не описаны: https://mmbr.asm.org/content/80/3/523.long
[21] GPMB): https://apps.who.int/gpmb/about.html
[22] Мир под угрозой: http://apps.who.int/gpmb/assets/annual_report/GPMB_annualreport_2019.pdf
[23] Источник: https://habr.com/ru/post/471562/?utm_source=habrahabr&utm_medium=rss&utm_campaign=471562
Нажмите здесь для печати.