То, каким является окружающий мир, зависит от того, как мы его воспринимаем. И дело не о психологии, а о сенсорике. Слух, зрение, прикосновение, вкус и запах — все эти чувства являются результатом совместной работы соответствующих органов чувств, собирающих сенсорную информацию, и , обрабатывающего ее. Нарушение работы одного из этих органов приводит к серьезным негативным последствиям для жизни любого живого существа. Потому понимание работы таких систем крайне важно. Ученые из Гарвардской медицинской школы (Бостон, штат Массачусетс, США) провели уникальное исследование обоняние, в котором установили, что рецепторы обоняния не располагаться «хаотично» в носу, а следуют четкому паттерну. Какие опыты проводили ученые, какие были получены данные, и что может нам рассказать карта обонятельных рецепторов? Ответы на эти вопросы мы найдем в докладе ученых.
Основа исследования
Нервная система использует пространство для отображения ощущений. Например, ушная улитка кодирует различные частоты в разных точках вдоль своей развернутой длины. Эта тонотопическая карта последовательно распространяется посредством структурированных проекций к стволу головного
Два препятствия затрудняют понимание того, имеют ли обонятельные сенсорные нейроны (OSN) пространственную структуру в эпителии. Во-первых, охарактеризовать взаимосвязь между физическим расположением и экспрессией генов в MOE сложно, поскольку лежащие в его основе хрящевые носовые раковины превращают гладкий и непрерывный эпителиальный сенсорный слой в сложный лабиринт, что затрудняет анализ пространственного порядка. Во-вторых, большая часть имеющихся знаний о пространственной структуре экспрессии обонятельных рецепторов получена с помощью гибридизации in situ и связанных с ней методов, которые обычно позволяют исследовать лишь несколько генов одновременно и которые трудно сопоставить между образцами. Хотя микродиссекция недавно использовалась для отнесения OR к определенным эпителиальным участкам, полученные оценки положения являются косвенными, и степень межиндивидуальной стереотипности остается неясной.
Изображение №1
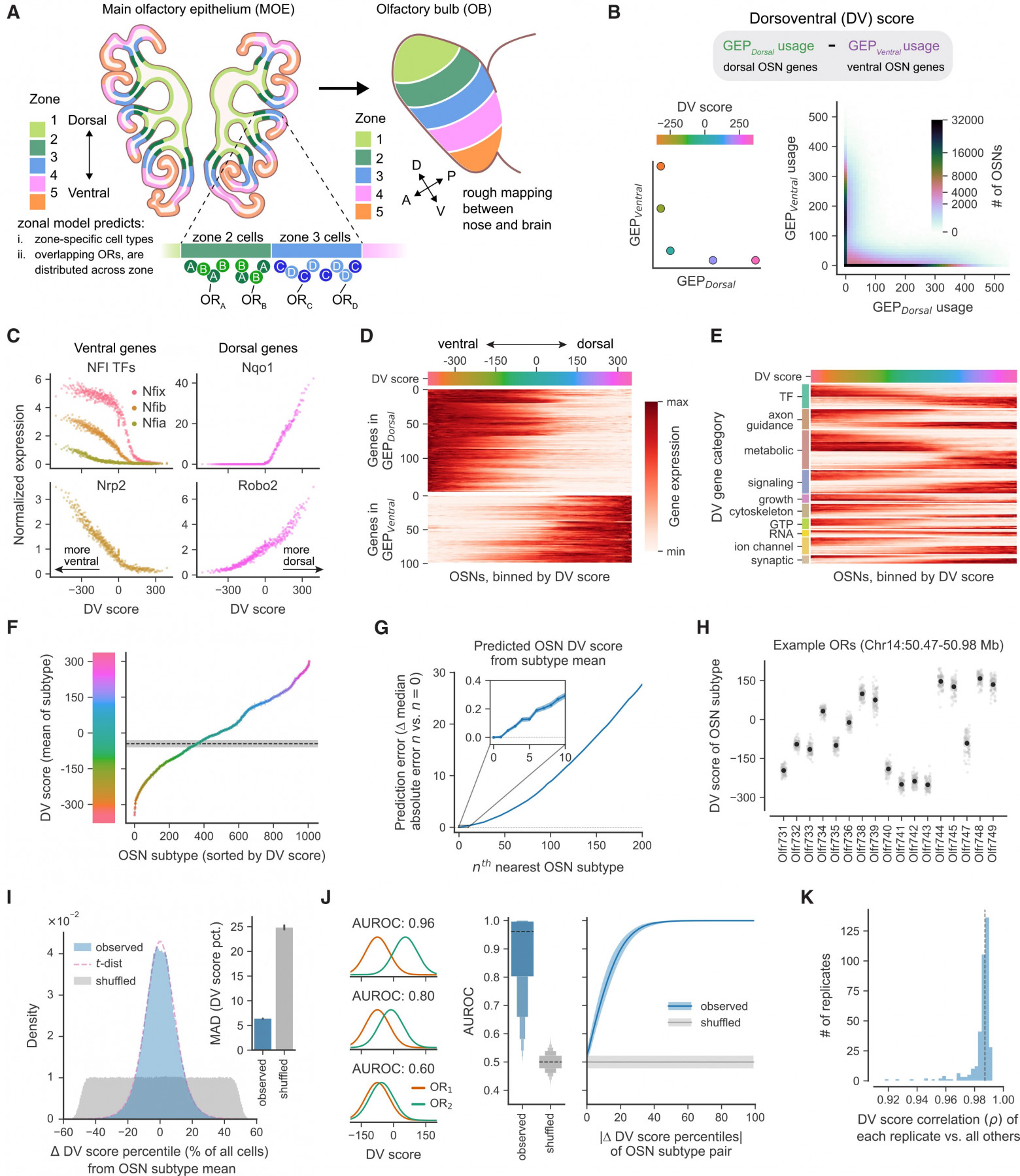
Несмотря на эти ограничения, современные модели предполагают, что отдельные рецепторы распределяются по одной из четырех-девяти дорсовентральных (DV от dorsoventral) «зон» (причем некоторые модели предполагают наличие дополнительных подзон), но выбираются обонятельными нейронами (OSN) случайным образом внутри каждой зоны, что приводит к пространственно распределенной экспрессии каждого обонятельного рецептора на обширной поверхности эпителия (1A). Поскольку MOE непрерывно регенерирует во взрослом возрасте из популяции базально локализованных стволовых клеток, эта зональная модель подразумевает, что предшественники OSN приобретают специфичные для каждой зоны клеточные идентичности, которые ограничивают выбор OR соответствующим подмножеством. В соответствии с этой возможностью, известно, что OSN разделяются на небольшое число линий с ограниченной судьбой, каждая из которых экспрессирует различный класс генов рецепторов. Предшественники OSN на поздних стадиях также, по-видимому, обречены на выбор из ограниченных подмножеств OR, поскольку «переключения» OR, иногда наблюдаемые во время дифференцировки OSN, в основном среди OR из одной и той же эпителиальной зоны. Однако лишь небольшое количество маркерных генов однозначно идентифицирует самую дорсальную зону, и не было выявлено ни одного гена, который бы разграничивал различные вентральные зоны.
Также остается неясным, как предшественники обонятельных нейронов могут ограничивать выбор обонятельных рецепторов пространственно подходящим набором из ~150–250 рецепторов на зону. Такие ограничения в конечном итоге должны влиять на механизмы, посредством которых предшественники выбирают один рецептор, которые еще не до конца изучены, но включают: низкий уровень совместной экспрессии рецепторов в предшественниках обонятельных нейронов, что может предоставлять рецепторам возможность потенциального выбора; подавление рецепторов, которые в конечном итоге не выбираются, посредством гетерохроматина; межхромосомные взаимодействия между генами рецепторов, которые способствуют как подавлению, так и выбору рецепторов; и, наконец, высокий уровень экспрессии одного аллеля рецептора. Эти механизмы выбора могут быть чувствительны к зональному положению, поскольку недавние результаты показывают, что зональное положение может влиять на набор рецепторов, доступных для совместной экспрессии в клетках-предшественниках.
Информация от обонятельных нейронов передается в островковые структуры, называемые гломерулами, в обонятельной луковице (OB от olfactory bulb), первом промежуточном звене в головном
В рассматриваемом нами сегодня труде учеными показано, что в носу находится карта рецепторов, построенная на основе примерно 1100 различимых пиков экспрессии обонятельных рецепторов (OR), средние положения которых надежно стереотипны у разных мышей. Эта закономерность является следствием согласованной транскрипционной программы, включающей около 250 генов, в том числе ключевые факторы транскрипции, компоненты сигнального пути ретиноевой кислоты (RA от retinoic acid) и молекулы, направляющие рост аксонов. Относительное использование этой программы отличает все зрелые подтипы обонятельных нейронов, систематически варьируется в зависимости от пространственного положения в эпителии и отражает градиенты RA в мезенхиме под собственно обонятельным эпителием. Стволовые клетки и предшественники обонятельных нейронов используют эту программу, которая влияет на многие известные механистические процессы, лежащие в основе выбора OR, и предсказывает пространственное расположение целевых клубочков, для кодирования информации о пространственном положении до выбора рецепторов для экспрессии и до начала процесса направленного роста аксонов. Таким образом, транскрипционная идентичность предшественников обонятельных нейронов определяется пространственно организованными градиентами экспрессии генов, которые затем преобразуются в дискретные и предсказуемые варианты выбора обонятельных рецепторов и гломерулярных мишеней; этот механизм координированно организует первые два этапа периферической обонятельной системы, создавая подробную карту рецепторов в носу, выровненную с точной картой рецепторов, наблюдаемой в обонятельной луковице.
Результаты исследования
Ученые предположили, что обонятельные нейроны содержат транскрипционные сигнатуры, отражающие их пространственное положение в эпителии. Для проверки этой идеи было использовано секвенирование РНК отдельных клеток (scRNA-seq) для характеристизации примерно 5 миллионов клеток MOE у сотен мышей, что позволило получить набор данных из примерно 2.3 миллионов обонятельных нейронов, которые в совокупности экспрессировали около 1100 обонятельных рецепторов.
Однако метод матричной факторизации позволил выявить несколько специфических для обонятельных нейронов программ экспрессии генов (GEP от gene expression program), каждая из которых состоит примерно из 100–200 отдельных генов, уровни экспрессии которых изменяются совместно в разных обонятельных нейронах. Две такие программы GEP (предварительно названные GEPDorsal и GEPVentral) включали гены, такие как известный дорсальный маркер Nqo1 и вентральные маркеры Nfia/b/x, которые кодируют семейство транскрипционных факторов ядерного фактора I (NFI от nuclear factor I); эти две программы GEP также включали множество дополнительных транскрипционных факторов, молекул, направляющих рост аксонов, и генов, регулирующих цитоскелет.
Для простоты ученые свели экспрессию генов, составляющих каждый GEP в каждой OSN, к одному числу — «использование» GEP. Поскольку отдельные OSN использовали либо GEPDorsal, либо GEPVentral, но не оба одновременно, ученые могли дополнительно обобщить использование этих двух GEP, вычислив показатель DV (т.е., использование GEPDorsal за вычетом использования GEPVentral) (1B). В отличие от того, что можно было бы ожидать, если бы OSN были организованы в однородные и дискретные «зоны», экспрессия Nqo1 тонически и плавно увеличивалась в зависимости от показателя DV каждой OSN, как и примерно 100 других генов, участвующих в GEPDorsal (включая, например, Robo2); Напротив, экспрессия Nfia/b/x и примерно 150 других генов, участвующих в GEPVentral (включая, например, Nrp2), тонически снижалась в зависимости от показателя DV каждого OSN (1C–1E). Таким образом, экспрессия примерно 250 генов, составляющих GEPDorsal и GEPVentral, систематически изменяется градуированным образом в разных OSN.
Использование GEPDorsal и GEPVentral данным обонятельным нейроном отражало экспрессируемый им обонятельный рецептор, поскольку каждый подтип обонятельного нейрона (определяемый как совокупность обонятельных нейронов, экспрессирующих один и тот же обонятельный рецептор) был связан с уникальным средним баллом DV; средние баллы DV плавно изменялись между подтипами без очевидной кластеризации (1F– 1H). Взаимосвязь между подтипами обонятельных нейронов и значениями DV отражала структурированную ковариацию между многими генами, поскольку значения DV хорошо аппроксимировались случайными подмножествами из 10–20 генов DV и мало изменялись после исключения дорсальных и вентральных маркерных генов. Отдельные обонятельные нейроны, принадлежащие к каждому подтипу, демонстрировали тесно связанные (но не идентичные) значения DV, так что обонятельные нейроны, принадлежащие к разным подтипам, могли быть эффективно различены только на основе их значений DV (1I, 1J). Способность различать подтипы обонятельных нейронов зависела от разницы в значениях DV каждой пары, как внутри, так и между предложенными зонами (1J). Аналогично, уровни экспрессии почти каждого гена DV лучше предсказывались значениями DV, чем предполагаемой зональной принадлежностью каждого подтипа.
Взаимосвязь между каждым подтипом OSN и соответствующим ему средним показателем DV была удивительно стабильной, поскольку ранжирование подтипов OSN на основе их показателей DV оставалось практически неизменным в сотнях независимых выборок (1K). Таким образом, несмотря на вариации показателей DV среди отдельных OSN, экспрессирующих один и тот же OR, средний показатель DV, связанный с каждым подтипом OSN, который суммирует скоординированную экспрессию нескольких сотен генов, является уникальным и стереотипным для всех мышей и достаточен для дифференциации каждого подтипа OSN от всех остальных.
Показатели DV предсказывают уникальное среднее пространственное положение каждого OR
Изображение №2
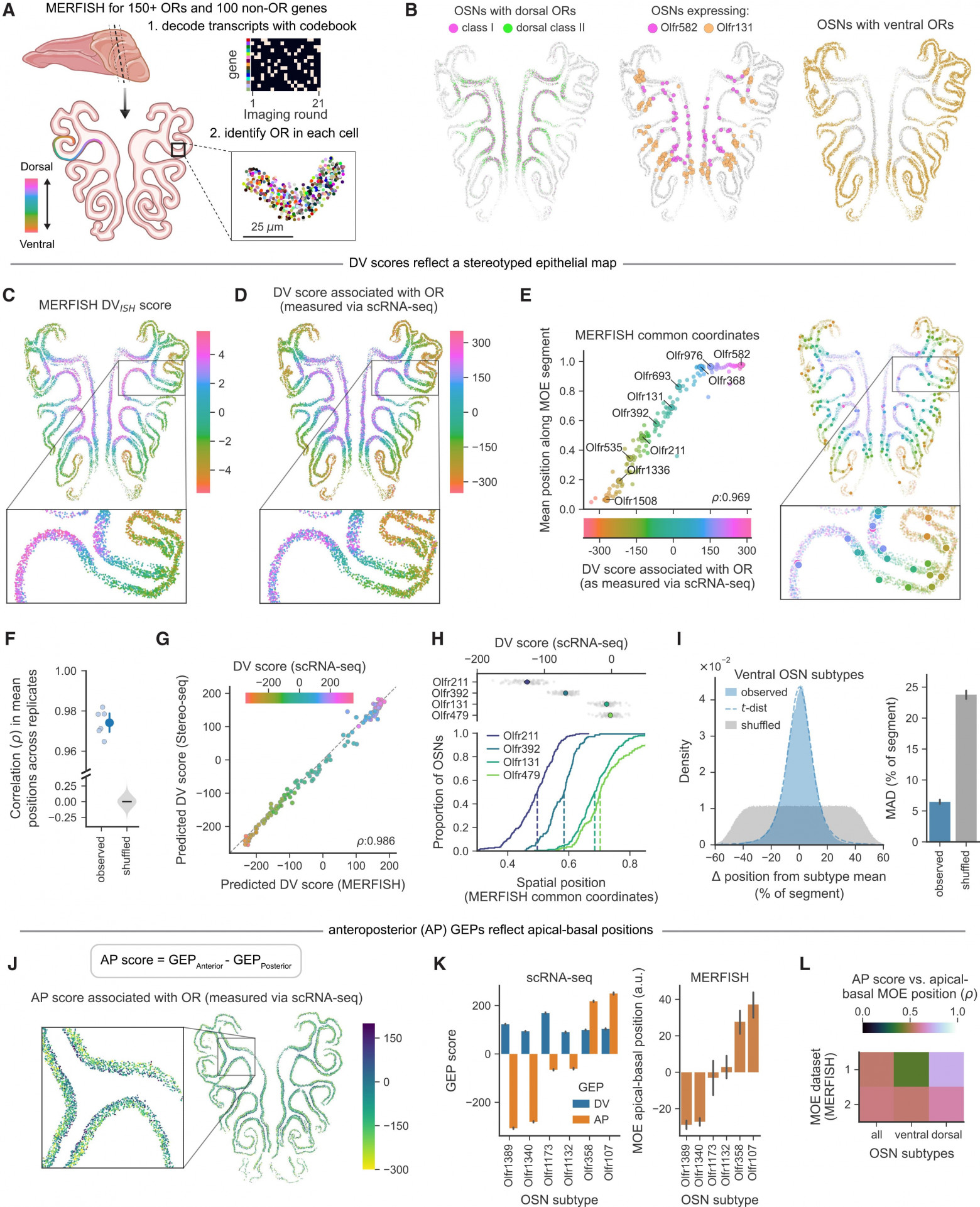
Ученые предположили, что точное DV-положение, занимаемое каждым OSN в эпителии, кодируется его показателем DV. Если это так, то среднее физическое положение каждого подтипа OSN — и, следовательно, OR — вдоль оси DV должно быть уникальным, предсказуемым и стереотипным для разных мышей. Чтобы проверить эту альтернативную гипотезу дискретной зональной модели, ученые использовали мультиплексную устойчивую к ошибкам флуоресцентную гибридизацию in situ (MERFISH от multiplexed error-robust fluorescence in situ hybridization) для измерения пространственного положения сотен генов OR и DV по всему эпителию (2A, 2B).
Как и ожидалось, отдельные обонятельные рецепторы экспрессировались в пространственно ограниченной форме, при этом наиболее дорсальные рецепторы экспрессировались шире, чем более вентральные (2B). Однако простое окрашивание каждого обонятельного нейрона на основе связанных с ним паттернов экспрессии генов DV (оценка DVISH, определенная непосредственно с помощью MERFISH) выявило ранее недооцененную тонкую организацию эпителия: вдоль каждого сегмента оценки DVISH плавно изменялись от дорсальной к вентральной плоскости (2C). Кроме того, идентификация OR, экспрессируемого в каждом OSN, и его окрашивание на основе его оценки DV (измеренной с помощью scRNA-seq) также дали аналогичный плавный и непрерывный пространственный градиент (2D). Физическое пространство также организовывало оценки OSN DV, когда эпителий был «развернут», выравнивая все сегменты по общей пространственной оси (2E). Учитывая, что каждый подтип OSN связан с уникальным средним значением DV-показателя, эти наблюдения показывают, что каждый OR занимает уникальное среднее положение вдоль DV-оси эпителия.
Плавные изменения взаимосвязи между положением эпителия, показателями DV и экспрессией OR сохранялись у разных животных и позволили точно предсказывать пространственное расположение каждого подтипа OSN (и, следовательно, OR) в данных MERFISH, в отдельном наборе данных пространственной транскриптомики, полученном с помощью Stereo-seq, и в пяти независимо полученных наборах данных, в которых положение подтипов OSN можно было точно или приблизительно определить (2F, 2G). В отличие от этого, не наблюдалось какой-либо дискретной пространственной кластеризации OR в четкие зоны, а показатели DV превосходили зональные модели в предсказании пространственного положения OSN.
В то время как вентральные подтипы обонятельных нейронов имели четко выраженные и предсказуемые средние местоположения, составляющие их обонятельные нейроны занимали распределение местоположений (с резким пиком и длинными хвостами, охватывающими ~5–15% эпителия), при этом степень перекрытия распределений оценок DV между подтипами обонятельных нейронов предсказывала степень их пространственного перекрытия (2H, 2I). Связь между пространственными положениями и оценками DV была менее очевидна в самой дорсальной области (2D, 2E), что, вероятно, отражает более широкое пространственное распределение, наблюдаемое для дорсальных рецепторов. Важно отметить, что оценки DVISH точно предсказывали пространственные положения внутри обонятельных нейронов данного подтипа, предполагая, что вариация оценок DV в значительной степени отражает различия в физическом местоположении, а не шум.
В совокупности эти данные показывают, что точное местоположение каждого обонятельного нейрона хорошо определяется его показателем DV, и что каждый подтип обонятельных нейронов занимает уникальное и ограниченное пространственное распределение в обонятельном эпителии, создавая таким образом карту рецепторов с примерно 1100 перекрывающимися, но различимыми пиками. Эта закономерность является следствием того, что каждый обонятельный рецептор имеет предпочтительное пространственное положение в эпителии, и что обонятельные нейроны, находящиеся в каждом пространственном положении, имеют предпочтительный обонятельный рецептор.
Показатели AP отражают апикально-базальное положение в эпителии
Метод факторизации выявил дополнительную пару GEP (в общей сложности около 300 генов), которые ученые предварительно назвали GEPAnterior и GEPPosterior, поскольку они включали гены (такие как Nrp1 и Plxna1), известные тем, что опосредуют направленное движение аксонов вдоль передне-задней (AP от anteroposterior) оси луковицы. Аналогично GEP DV, OSN использовали либо GEPAnterior, либо GEPPosterior, что позволило сгенерировать «показатель AP», который варьировался в зависимости от подтипа. Ученіе задались вопросом, обусловлена ли эта вариация также расположением в эпителии, и с помощью MERFISH наблюдалось, что различия в показателях AP между подтипами OSN соответствовали их апикально-базальному положению в слое OSN (2J, 2K). Эта взаимосвязь была наиболее выражена для дорсальных подтипов OSN (2L), которые, что примечательно, представляют собой подгруппу OSN, в которой показатели DV наименее информативны относительно пространственного положения.
Идентичность DV не зависит от экспрессируемого OR и последующей активности
Предыдущие исследования показывают, что спонтанная активность, специфичная для OR, определяет экспрессию некоторых генов AP GEP. Поэтому ученые задались вопросом, определяется ли оценка DV каждого подтипа OSN аналогично экспрессируемым OR. Чтобы проверить эту идею, было проведено scRNA-seq на OMP-IRES-tTA; tetO-P2 (OMP-P2) мышах, у которых рецептор P2 эктопически экспрессируется по оси DV; этот процесс часто подавляет ранее выбранный OR в каждом OSN. OSN P2 от мышей OMP-P2 имели гораздо более широкое распределение оценок DV, чем OSN, экспрессирующие P2, от мышей дикого типа; этот результат демонстрирует, что идентичность (и связанная с ней активность) экспрессируемого OR не определяет оценки DV OSN, предполагая вместо этого, что оценки DV определяются пространственным положением OSN. В соответствии с этой альтернативной гипотезой, примерно 15% обонятельных нейронов, в которых P2 экспрессировался совместно с другим обонятельным рецептором (т. е., которые переключались со своего исходного рецептора на P2), демонстрировали показатели DV, которые соответствовали исходно выбранному рецептору, а не P2. Активность, вызванная запахом, ниже по течению от рецептора, также, по-видимому, вряд ли определяла показатели DV, которые практически не изменились после трех различных манипуляций с активностью: окклюзии ноздрей, воздействия новой обонятельной среды и нокаута CNGA2, ключевого ионного канала, который преобразует активацию рецептора в поступление кальция и импульсную активность. Таким образом, рецептор, экспрессируемый каждым обонятельным нейроном, не влияет на его показатель DV, тем не менее в нормальных условиях идентичность экспрессируемого рецептора коррелирует с пространственным положением каждого обонятельного нейрона и показателем DV.
Транскрипционные признаки идентичности DV присутствуют в предшественниках OSN
Изображение №3
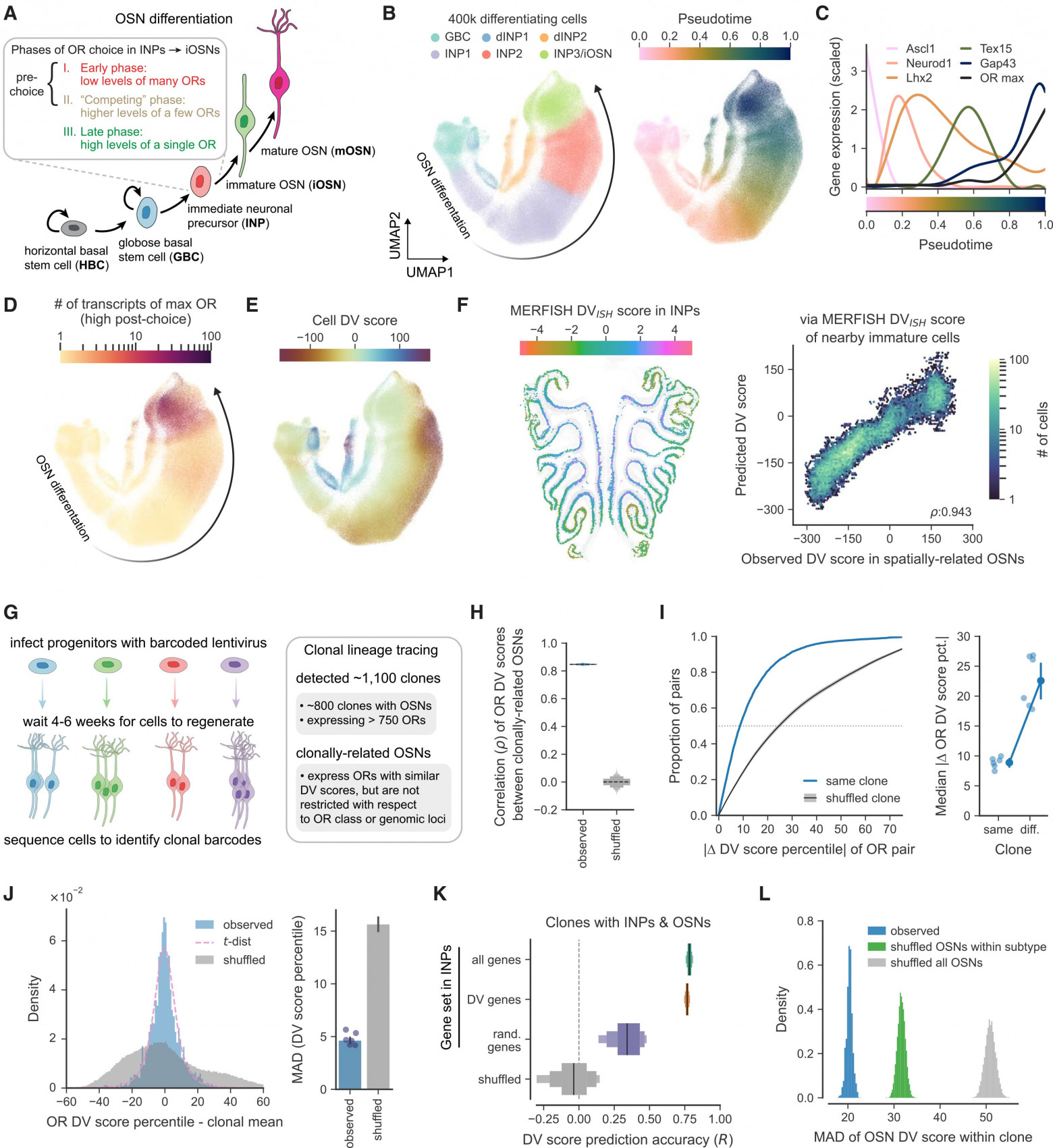
Эти наблюдения предполагают модель, в которой пространственно организованные паттерны экспрессии генов DV инициируются до экспрессии OR либо в стволовых клетках, либо в непосредственных нейрональных предшественниках (INP от immediate neuronal precursor), которые находятся в организованных слоях под их зрелыми потомками (3A). Для проверки этой гипотезы ученые проанализировали экспрессию генов DV в 400000 дифференцирующихся клетках, извлеченных из набора данных scRNA-seq (3B–3D). Многие гены DV экспрессировались во время дифференцировки OSN, что позволило вычислить показатели DV для всех клеток-предшественников. Это выявило градиент значений DV среди предшественников OSN, который присутствовал на всех стадиях дифференцировки и охватывал все три линии OSN (соответствующие экспрессии обонятельных рецепторов класса I, дорсальных обонятельных рецепторов класса II и вентральных обонятельных рецепторов класса II), что очевидно в используемом наборе данных (3E).
Анализ главных компонентов показал, что вариация значений DV является основным фактором транскрипционной вариации среди предшественников на каждой стадии развития, хотя экспрессия отдельных генов DV достигала пика на разных стадиях. Различия в экспрессии генов DV у предшественников отражали различия в пространственном расположении внутри эпителия, в то время как в каждом месте DV предшественники и расположенные над ними OSN демонстрировали схожие значения DV (3F). Таким образом, пространственное положение определяет уровни экспрессии генов GEPDorsal и GEPVentral на всех стадиях дифференцировки обонятельных нейронов, тем самым транскрипционно диверсифицируя предшественники обонятельных нейронов до того, как они примут решение об экспрессии единственного обонятельного рецептора.
Клонально связанные клетки экспрессируют ограниченные наборы OR со схожей идентичностью домена DV
Наблюдение, что предшественники и расположенные рядом обонятельные нейроны имеют схожие значения домена DV, предполагает, что положение домена DV стволовой клетки может ограничивать выбор OR. Для проверки этой идеи ученые провели отслеживание клональных линий in vivo, химически аблатируя OSN метимазолом и интраназально инфицируя базальные стволовые клетки лентивирусными ДНК-штрихкодами. После того как стволовым клеткам дали возможность регенерировать эпителий в течение нескольких недель, было проведено секвенирование РНК отдельных клеток (scRNA-seq) для идентификации набора подтипов OSN (и, следовательно, OR), генерируемых каждой помеченной стволовой клеткой (3G).
Большинство идентифицированных клонов (около 800 из ~1100) включали обонятельные нейроны, которые в совокупности экспрессировали более 750 различных OR. Отдельные OSN, полученные из одного и того же клона, часто экспрессировали разные OR, что демонстрирует отсутствие детерминированной связи 1:1 между позиционной идентичностью стволовой клетки и выбором OR. Однако клонально связанные OSN имели гораздо более схожие показатели DV, чем OSN из разных клонов, и, как следствие, экспрессировали один и тот же OR с частотой выше случайной (3H–3J). Клонально связанные предшественники также имели схожие показатели DV; что важно, экспрессия генов DV предшественников может быть использована для прогнозирования OR, экспрессируемых OSN, обнаруженными в одном и том же клоне (определяемых по соответствующим показателям DV) (3K). Интересно, что показатели DV у клонально связанных OSN были даже более ограниченными, чем ожидалось, исходя из выбранных ими OR, что предполагает более тесную связь между эпителиальным пространством и идентичностью DV, чем между эпителиальным пространством и выбором OR (3L). Эти наблюдения согласуются с тем, что процесс выбора OR у предшественников OSN смещен в сторону пространственно оптимального рецептора, тем самым создавая упорядоченную карту идентичности OR в носу, но также достаточно стохастичен, так что предшественники OSN часто выбирают OR, связанные с подтипами OSN, расположенными близко в пространстве.
Сигнализация RA варьируется в пространстве и влияет на выбор OR.
Изображение №4
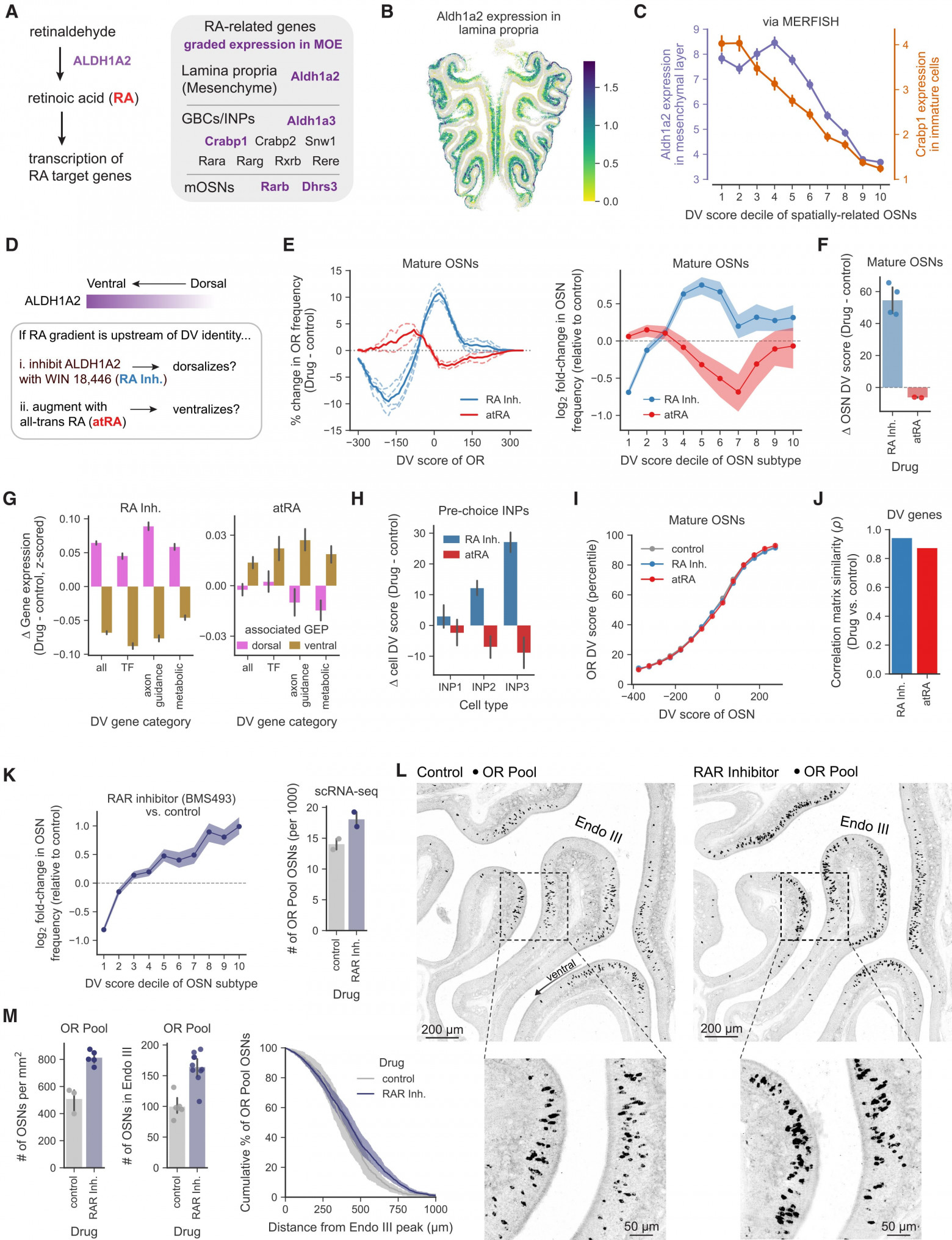
Результаты показывают, что предшественники OSN каким-то образом «знают», где они физически расположены вдоль оси DV, что позволяет выбирать OR с учетом местоположения. В соответствии с этой идеей, обонятельные нейроны, регенерированные после обработки метимазолом, демонстрировали те же взаимосвязи между показателями DV и выбором OR, которые наблюдались в необработанном эпителии. Ученые искали потенциальные сигнальные программы, которые могли бы информировать стволовые клетки об их положении DV, и обнаружили несколько генов, связанных с сигнализацией RA, экспрессия которых варьировалась в пространстве в разных типах эпителиальных клеток (4A). В соответствии с предыдущими исследованиями, ретинальдегиддегидрогеназа 2 (ALDH1A2, фермент, который превращает ретинальдегид в RA) экспрессируется в мезенхимальных клетках собственной пластинки — ниже слоя стволовых клеток — в градиенте, который отрицательно коррелировал с показателями DV близлежащих подтипов обонятельных нейронов (4B, 4C). Предшественники обонятельных нейронов экспрессировали рецепторы ретиноевой кислоты (RA), такие как Rara, Rarg, Rxrb и Rere, а предшественники и обонятельные нейроны экспрессировали дополнительные гены, способные продуцировать RA или реагировать на нее градуированным образом, включая Aldh1a3, Rarb, Dhrs3 и клеточный белок 1, связывающий RA (Crabp1) (4A, 4C).
Таким образом, мезенхимальная ретиноевая кислота (RA) может сигнализировать о положении DV и влиять на судьбу обонятельных нейронов (OSN). Для проверки этой гипотезы ученые системно вводили взрослым мышам либо ингибитор ALDH1A2 (WIN 18,446), либо активатор RA-сигнализации (полностью транс-ретиновая кислота [atRA]) во время регенерации, индуцированной метимазолом, и оценивали их эффекты с помощью scRNA-seq (4D). По сравнению с контрольными мышами наблюдались двунаправленные сдвиги в количестве регенерированных «дорсальных» или «вентральных» OSN: у мышей, получавших ингибитор RA, было относительно меньше OSN с более вентральными показателями DV (и, следовательно, меньше клеток, экспрессирующих вентральные обонятельные рецепторы), тогда как у мышей, получавших atRA, наблюдался противоположный фенотип (4E); эти двунаправленные, RA-зависимые сдвиги в показателях DV наблюдались как в предшественниках, так и в OSN (4F–4H). Важно отметить, что эти манипуляции не изменили взаимосвязь между показателями DV и выбранными OR как таковыми, а также не изменили структуру ковариации генов, составляющих показатель DV (4I и 4J). Маловероятно, что побочные эффекты лекарственных препаратов объясняют эти наблюдения, поскольку лечение мышей обратным агонистом пан-ретиноидного рецептора (RAR от retinoic acid receptor) (BMS493) также привело к сдвигам в сторону дорсального направления в выборе OR и показателях DV (4K).
Эти результаты предсказывают, что ингибирование сигнализации RA должно сместить относительное положение подтипов OSN вдоль дорсовентральной оси эпителия, что ученые проверили, проведя гибридизацию in situ для объединенного набора OR, экспрессируемых в дорсальной части вентрального эпителия. В соответствии с результатами scRNA-seq, обработка BMS493 привела к тому, что больше клеток экспрессировали относительно дорсальные OR; кроме того, пространственное распределение этих клеток сместилось вентрально (4L и 4M). Это согласуется с тем, что вентральный эпителий дорсализируется в условиях ингибирования RA.
Связь расположения DV с OR выбором
Данные свидетельствуют о том, что субэпителиальный градиент ретиноевой кислоты информирует вышележащие стволовые клетки и предшественники об их положении в дорсовентральном слое, тем самым преобразуя пространственное расположение в определенный паттерн экспрессии генов DV и, в конечном итоге, в выбор пространственно подходящих обонятельных рецепторов. Поэтому ученые задались вопросом, как экспрессия генов DV у предшественников может влиять на множественные механизмы, поддерживающие выбор одного OR, которые в общих чертах включают низкоуровневую коэкспрессию множества рецепторов, подавление невыбранных рецепторов посредством направленной гетерохроматинизации и геномной компартментализации генов обонятельных рецепторов, а также селективную высокоуровневую экспрессию одного гена обонятельного рецептора.
Совместная экспрессия рецепторов организована вдоль дорсально-венозного градиента
Изображение №5
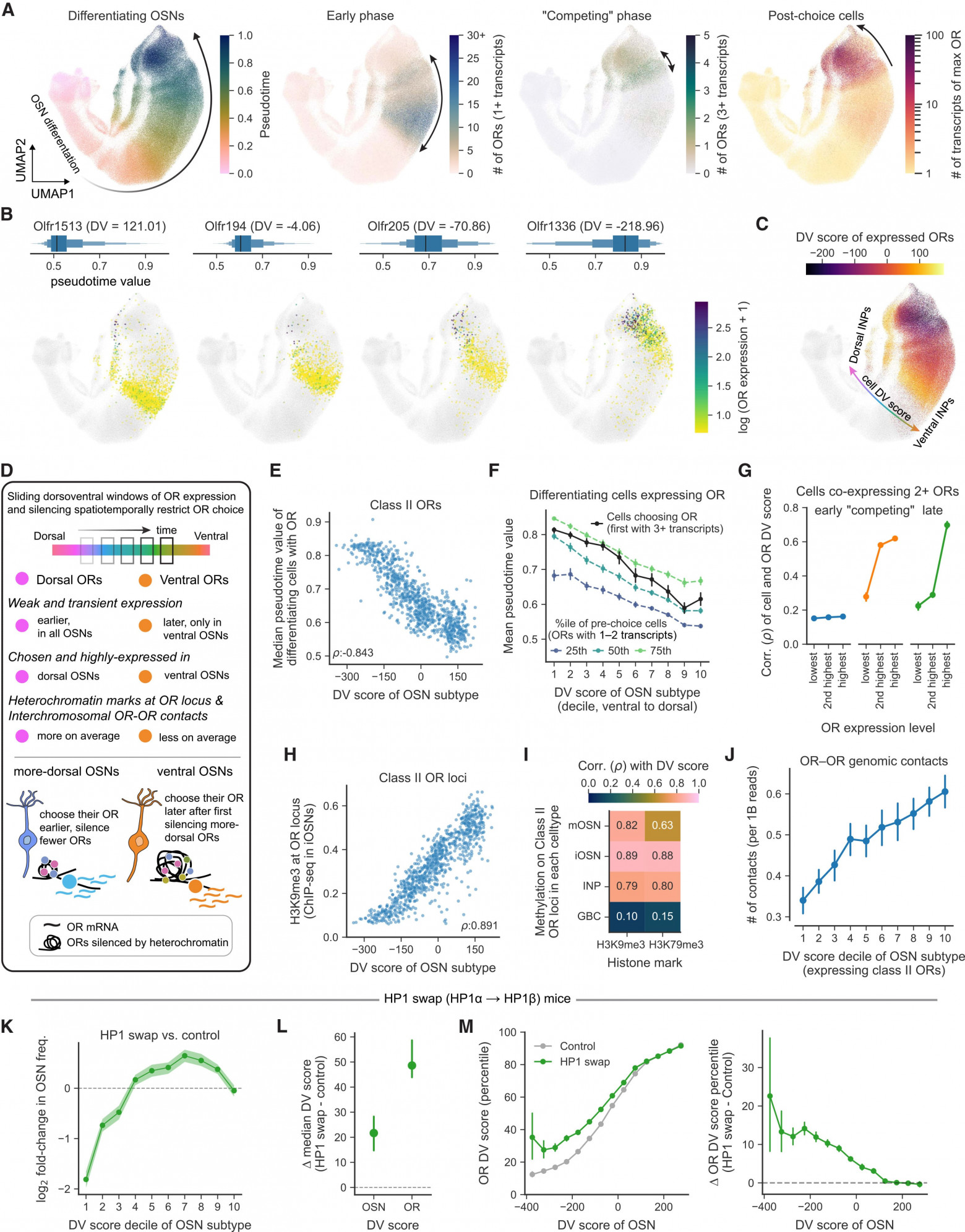
Псевдовременная упорядоченность данных scRNA-seq подтвердила, что предшественники обонятельных нейронов часто совместно экспрессируют 10–20 рецепторов обоняния на низком уровне, прежде чем в конечном итоге выберут один рецептор для экспрессии на высоком уровне. Ученые задались вопросом, преимущественно ли совместно экспрессируются дорсальные рецепторы у предшественников дорсальных нейронов, и наоборот, совместно ли совместно экспрессируются вентральные рецепторы у предшественников вентральных нейронов. Удивительно, но все предшественники, независимо от пространственного положения (определяемого по DV показателю каждой клетки), первоначально экспрессируют ограниченное подмножество самых дорсальных рецепторов (5A–5C). Впоследствии самые дорсальные предшественники экспрессируют дорсальные рецепторы обоняния на более высоком уровне, так что дорсальные рецепторы обоняния, такие как Olfr1513, экспрессируются исключительно на высоком уровне в дорсальных клетках.
Напротив, более вентральные предшественники, наоборот, подавляют слабо коэкспрессируемые дорсальные OR и начинают коэкспрессировать несколько более вентральные OR, такие как Olfr194 (5B). По мере развития дифференцировки эти предшественники аналогичным образом разрешают свою коэкспрессию в единый выбор, и процесс коэкспрессии, отбора (если это пространственно уместно) и подавления (если нет) постепенно повторяется в дорсально-вентральном направлении, пока наиболее вентральные OR, наконец, не начнут коэкспрессироваться и впоследствии выбираться в наиболее вентральных клетках.
В результате этого процесса возникает скользящее окно совместной экспрессии OR, которое систематически изменяется по мере дифференциации предшественников обонятельных нейронов: сначала совместно экспрессируются и выбираются рецепторы, расположенные в самой дорсальной части, а затем – рецепторы, расположенные в самой вентральной части (5C–5F). Задержка между выбором дорсальной и вентральной частей, вероятно, отражает тот факт, что вентральные клетки-предшественники должны сначала совместно экспрессировать и подавлять экспрессию большего количества дорсальных OR, прежде чем они смогут экспрессировать пространственно подходящий вентральный OR. Следует отметить, что рецепторы класса I, расположенные в самой дорсальной зоне, нарушают эту закономерность совместной экспрессии и подавления. Это согласуется с тем, что обонятельные нейроны, экспрессирующие OR класса I, имеют отдельную траекторию развития.
Предсказывают ли пространственные характеристики каждого предшественника OSN, какой из совместно экспрессируемых OR будет выбран для одиночной экспрессии? Ученые обнаружили, что на ранних стадиях дифференцировки наблюдается лишь слабое соответствие между слабо совместно экспрессируемыми OR и клеточными DV-показателями, но как только предшественники начинают экспрессировать OR на более высоких уровнях, единственный наиболее экспрессируемый OR становится хорошо согласован с клеточными DV-показателями (5G). Таким образом, по мере перехода предшественников OSN от экспрессии множественных к одиночным OR, уровни экспрессии «неправильных» OR систематически снижаются, в результате чего образуется OSN, который в среднем экспрессирует наиболее подходящий OR для своего заданного пространственного положения (хотя OSN по-прежнему часто выбирают OR, связанные с близлежащими пространственными позициями). В соответствии с тем, что градиенты RA информируют предшественники OSN о пространственном расположении, манипуляции с RA систематически смещали набор OR, которые совместно экспрессировались в клетках, находящихся на стадии предварительного выбора. Таким образом, позиционирование DV влияет не только на то, какой из ~1100 различных OR выбирает для экспрессии данный OSN, но и на то, как этот процесс разворачивается во время дифференцировки.
Градиент гетерохроматина подавляет неподходящую экспрессию OR
Гены OR, не выбранные для индивидуальной экспрессии, подавляются гетерохроматином, который откладывается на локусах OR во время дифференцировки. Ученые задались вопросом, могут ли регуляторы этого процесса участвовать в установлении взаимосвязей между показателями DV предшественников, временем выбора OR во время дифференцировки и набором OR, доступных для индивидуального выбора. Действительно, в недавних исследованиях было установлено, что транскрипционные факторы NFI причинно ответственны за регулирование уровня гетерохроматинизации обонятельных рецепторов в более вентральных зонах, поскольку нокаутирование генов Nfi в предшественниках обонятельных нейронов снижает уровень гетерохроматина на вентральных локусах обонятельных рецепторов и приводит к тому, что обонятельные нейроны в предполагаемых вентральных зонах экспрессируют больше дорсальных обонятельных рецепторов. Гены Nfi также, вероятно, связывают пространственную идентичность с выбором обонятельного рецептора, поскольку они являются частью GEPVentral, экспрессируются в дорсовентральном градиенте как в предшественниках, так и в обонятельных нейронах, и двунаправленно чувствительны к манипуляциям с RA (1C). Таким образом, экспрессия Nfi и, возможно, других регуляторных дорсовентральных генов, отражающих дорсовентральное положение, может напрямую влиять на процесс выбора в предшественниках обонятельных нейронов, регулируя отложение гетерохроматина пространственно-чувствительным образом.
Учитывая эти наблюдения, ученые выдвинули гипотезу, что отложение гетерохроматина в обонятельных нейронах может не различаться по зонам, а быть организовано в непрерывный дорсально-вентральный градиент, способный подавлять субоптимальные обонятельные нейроны, позволяя каждому предшественнику экспрессировать пространственно подходящие обонятельные нейроны. Для проверки этой идеи ученые повторно проанализировали наборы данных, в которых обонятельные нейроны из всего эпителия были объединены, а уровни гетерохроматиновых меток на каждом локусе обонятельного нейрона были количественно определены с использованием хроматиновой иммунопреципитации с последующим секвенированием ДНК (ChIP-seq). Если дифференцировка обонятельных нейронов требует гетерохроматинизации совместно экспрессируемых обонятельных нейронов — и наиболее дорсальные обонятельные нейроны экспрессируются транзиторно, а затем подавляются во всех предшественниках, тогда как вентральные обонятельные нейроны экспрессируются только в вентральных предшественниках, — то дорсальные локусы обонятельных нейронов должны иметь относительно более высокие уровни гетерохроматиновых меток в этом типе объединенного анализа.
Действительно, наблюдалась сильная монотонная зависимость между показателем DV, связанным с каждым OR, и уровнем гетерохроматина, наблюдаемым в его локусе (5H и 5I). В отличие от этого, в данных ChIP-seq от обонятельных нейронов, экспрессирующих вентральный рецептор Olfr1507, наблюдались относительно однородные уровни гетерохроматина по всем локусам OR. Это согласуется с тем, что вентральные обонятельные нейроны подавляют все более дорсальные локусы OR. Также наблюдался непрерывный градиент DV межхромосомных геномных контактов OR-OR, в котором дорсальные локусы OR систематически взаимодействуют с другими локусами OR чаще, чем вентральные локусы OR, при анализе в совокупности по всем обонятельным нейронам (5J). Этот результат предполагает, что в более вентральных обонятельных нейронах ядра имеют относительно больше межхромосомных геномных контактов между обонятельными рецепторами, чем в более дорсальных обонятельных нейронах, вероятно, потому что в них подавлено больше локусов обонятельных рецепторов. Таким образом, как и в случае с паттернами экспрессии обонятельных рецепторов, уровни гетерохроматина в локусах обонятельных рецепторов и геномные контакты между ними не организованы зонально, а систематически изменяются вдоль дорсовентрального градиента (5D).
Если уровни гетерохроматина регулируют выбор OR для экспрессии в данной пространственной позиции, то нарушение гетерохроматина может изменить взаимосвязь между пространственной позицией и выбором OR. Одна из стратегий для этого основана на обнаружении того, что гетерохроматинизированные локусы OR связываются с белком гетерохроматина 1β (HP1β), который помогает компактировать ДНК в ее репрессированную форму. Поскольку потеря HP1β приводит к неонатальной летальности, ученые провели scRNA-seq на мышах с «заменой HP1», у которых потеря HP1β компенсируется HP1α, который также взаимодействует с хроматином, но играет менее заметную роль в подавлении транскрипции.
OSN HP1-swap мышей были дорсализованы по сравнению с контрольными мышами и имели меньшее количество OSN, экспрессирующих вентральные рецепторы, аналогично тому, что ранее наблюдались после обработки мышей препаратами, снижающими передачу сигналов RA (5K). Однако, в отличие от того, что наблюдалось после манипуляций с RA, OSN и предшественники, полученные от HP1-swap мышей с заданным показателем DV, экспрессировали даже больше дорсальных рецепторов, чем можно было бы ожидать (5L, 5M). Тот факт, что эти манипуляции изменяют типичную взаимосвязь между экспрессией генов DV и выбором обонятельного рецептора, демонстрирует, что гетерохроматинизация OR — результат действия генов DV, таких как Nfi — причинно преобразует пространственное положение в пространственно соответствующее распределение обонятельных рецепторов.
Геномный контекст связывает пространственное положение с соответствующим выбором OR
Хотя вариации в уровнях гетерохроматина в локусах OR представляют собой убедительный способ подавления экспрессии пространственно неподходящих рецепторов, остается неясным, как каждый OR связан со своим конкретным пространственным положением. Одна из возможностей заключается в том, что различия в связывании и/или активности транскрипционных факторов, расположенных выше генов OR организуют экспрессию OR в пространстве. Анализ обогащения мотивов подтвердил наличие предполагаемых сайтов связывания для транскрипционных факторов LHX и EBF в большинстве промоторов OR. В соответствии с ранней экспрессией дорсальных OR во время дифференцировки обонятельных нейронов, OR с увеличенным числом сайтов связывания для EBF (который необходим для экспрессии OR) с большей вероятностью располагались дорсально. Кроме того, мотивы для транскрипционных факторов NFI и RAR были обогащены в промоторах более вентральных обонятельных нейронов, что согласуется с градиентной экспрессией как генов Nfi, так и генов, связанных с RA, наблюдаемой в вентральных OSN.
Эти наблюдения позволяют предположить, что локальный геномный контекст делает каждый OR способным к экспрессии в определенном DV-локусе в эпителии. Действительно, анализ мышей с «заменой рецепторов», у которых кодирующая последовательность одного рецептора заменяет последовательность другого рецептора в другом геномном локусе, показал, что показатели OSN DV (и уровни экспрессии Nfi и других генов DV) отражают геномный локус, в котором находится экспрессируемый OR.
Изображение №6
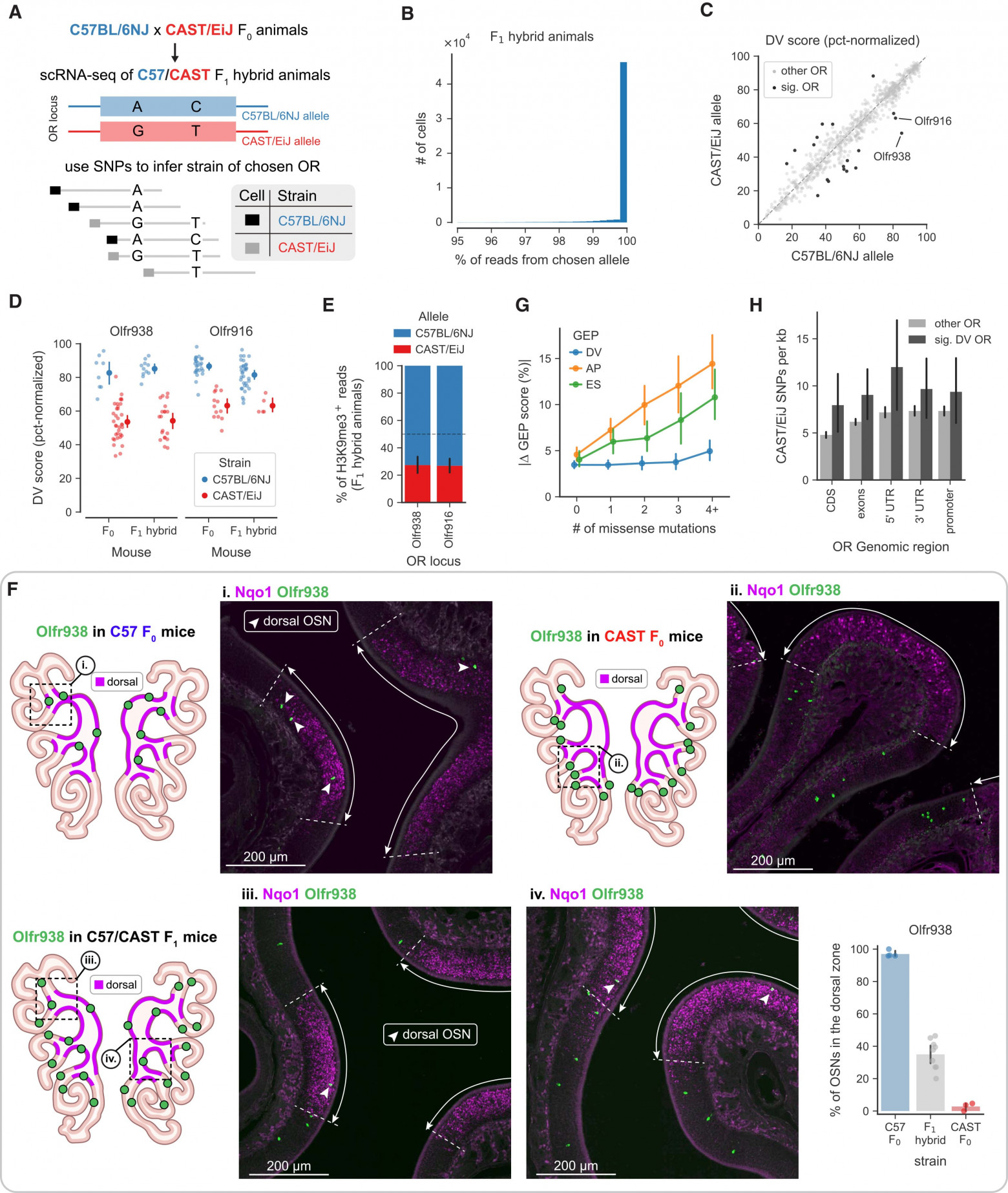
Для дальнейшего изучения достаточности цис-регуляторных элементов в определении позиционирования OR DV ученые охарактеризовали показатели DV в OSN из гибридных скрещиваний F1 между мышами C57BL/6J (C57) и мышами дикого типа CAST/EiJ (CAST) (6A). В соответствии с моноаллельной экспрессией генов OR, каждый OSN экспрессировал исключительно либо аллель C57, либо аллель CAST выбранного им OR (6B). Хотя эти два штамма мышей имеют в основном гомологичные наборы OR, их геномы также содержат множество однонуклеотидных полиморфизмов (SNP от single-nucleotide polymorphism), которые в принципе могут влиять на цис-регуляторные элементы и тем самым изменять пространственное положение OR.
В соответствии с этим предсказанием, подгруппа подтипов OSN (и, следовательно, подгруппа аллелей OR) продемонстрировала значительные межштаммовые различия в показателях DV как у гибридных мышей F1, так и у родительских штаммов F0 C57 и CAST (6C*). Ученые задались вопросом, могут ли эти штамм-специфические различия в показателях DV надежно предсказывать различия в эпителиальном положении отдельных OR. Поэтому была проведена гибридизация in situ для Olfr938 и Olfr916, двух OR с более высокими показателями DV и, соответственно, более высокими уровнями гетерохроматина у мышей C57 по сравнению с мышами CAST (6D и 6E). В соответствии с наблюдаемыми различиями в их показателях DV, обонятельные нейроны, экспрессирующие Olfr938 и Olfr916, располагались исключительно в дорсальной области Nqo1+ эпителия у мышей C57 и в вентральной области Nqo1− у мышей CAST (6F). Кроме того, исследование in situ для Olfr938 и Olfr916 у гибридов F1 показало, что один и тот же обонятельный рецептор находился как внутри, так и вне дорсальной области Nqo1+, и, таким образом, фактически располагался одновременно в двух «зонах», что соответствовало пространственному положению соответствующих F0 особей (6F).
Как геномные вариации OR могут приводить к пространственным вариациям между штаммами? Геномные SNP расположены как в вышележащих, так и в кодирующих областях генов OR. Однако ни специфические для штаммов мутации в кодирующих областях OR, ни количество SNP в вышележащих областях не предсказывали, будет ли положение данного OR варьироваться между штаммами (6G и 6H). Это предполагает, что конкретный набор вышележащих SNP определяет их влияние на пространственное положение. Действительно, сравнение пространственной картины экспрессии Olfr938 у мышей линий CAST, C57 и двух дополнительных диких линий (MOLF/EiJ и PWK/PhJ) с набором SNP, присутствующих в каждой линии, позволило выявить единственный вышележащий SNP как потенциально причинный фактор его вентральной экспрессии у мышей линии CAST. Этот анализ, в сочетании с экспериментами по генетическим манипуляциям и гибридизации F1, свидетельствует о том, что пространственное положение каждого OR определяется некодирующими элементами в его геномном локусе.
Филогения, функция и пространственное расположение слабо связаны
OR являются продуктом событий дупликации генов, которые могут генерировать гены OR с похожими промоторами и первичными последовательностями в близлежащих геномных локусах. Это явление предполагает, что геномное положение OR, филогенетические связи и/или химические свойства настройки могут коррелировать с показателями DV и, следовательно, с пространственным положением. В соответствии с предыдущими работами, предполагавшими, что гомологичные OR в пределах геномного кластера могут иметь схожую зональную идентичность, ученые обнаружили, что геномно смежные локусы OR имеют в среднем более схожие белковые последовательности (измеряемые их филогенетическим сходством) и более схожие эпителиальные пространственные положения (отражаемые показателем DV), чем более отдаленные локусы. Однако общая взаимосвязь между филогенетическим расстоянием и показателями DV была слабой. Это позволяет предположить, что эти эффекты могут наблюдаться лишь для небольшой подгруппы OR, например, для тех, которые являются недавними продуктами дупликации генов.
Хотя филогения OR лишь незначительно связана с пространственным положением, остается вероятность того, что сами свойства настройки OR пространственно организованы в эпителии. Для проверки этой возможности ученые использовали Act-seq для идентификации набора OSN, активируемых различными мономолекулярными одорантами, и для выявления связанных с ними OR и показателей DV. Мономолекулярные запахи, подаваемые в концентрациях, активирующих множество рецепторов, вызывали паттерны нейронной активации, пространственно распределенные по всему эпителию. В отличие от этого, кислоты в основном активировали OR класса I в дорсальной области эпителия, а запахи, подаваемые в концентрациях, активирующих меньшее количество OR, как правило, задействовали OR, которые в среднем имели более схожие показатели DV. Однако эта пространственная кластеризация свойств настройки запахов была слабой и, по-видимому, в значительной степени обусловлена тесными филогенетическими связями между подмножеством OR. Эти результаты показывают, что обонятельные рецепторы с очень похожими последовательностями иногда могут быть одновременно и настроены аналогично, и расположены близко друг к другу в эпителии, но в целом запахи активируют обонятельные нейроны, пространственно распределенные по всему эпителию.
Пространственное положение эпителиальных клеток координирует нацеливание аксонов в обонятельной луковице
Обонятельная луковица (OB) содержит точную и стереотипную карту, в которой каждый подтип обонятельных нейронов обычно проецируется в один медиальный и один латеральный клубочек. Помимо генов транскрипционных факторов, таких как Nfi и Rar, которые, вероятно, влияют на выбор OR, показатель DV включает известные регуляторы аксональной направленности обонятельных нейронов, такие как Robo2 и Nrp2, а также более тридцати дополнительных молекул клеточной поверхности и цитоскелета, которые могут способствовать направленному росту аксонов (например, Ncam1, Plxna4, Plxnb3, Cdh3). Поскольку экспрессия генов показателя DV не зависит от активности OR, часто предшествует выбору OR и изменяется в обоих направлениях при манипуляциях с сигнализацией ретиноевой кислоты, DV GEP представляют собой потенциально экономный механизм для связи эпителиального пространства как с процессом выбора OR, так и с направленным ростом аксонов.
Изображение №7
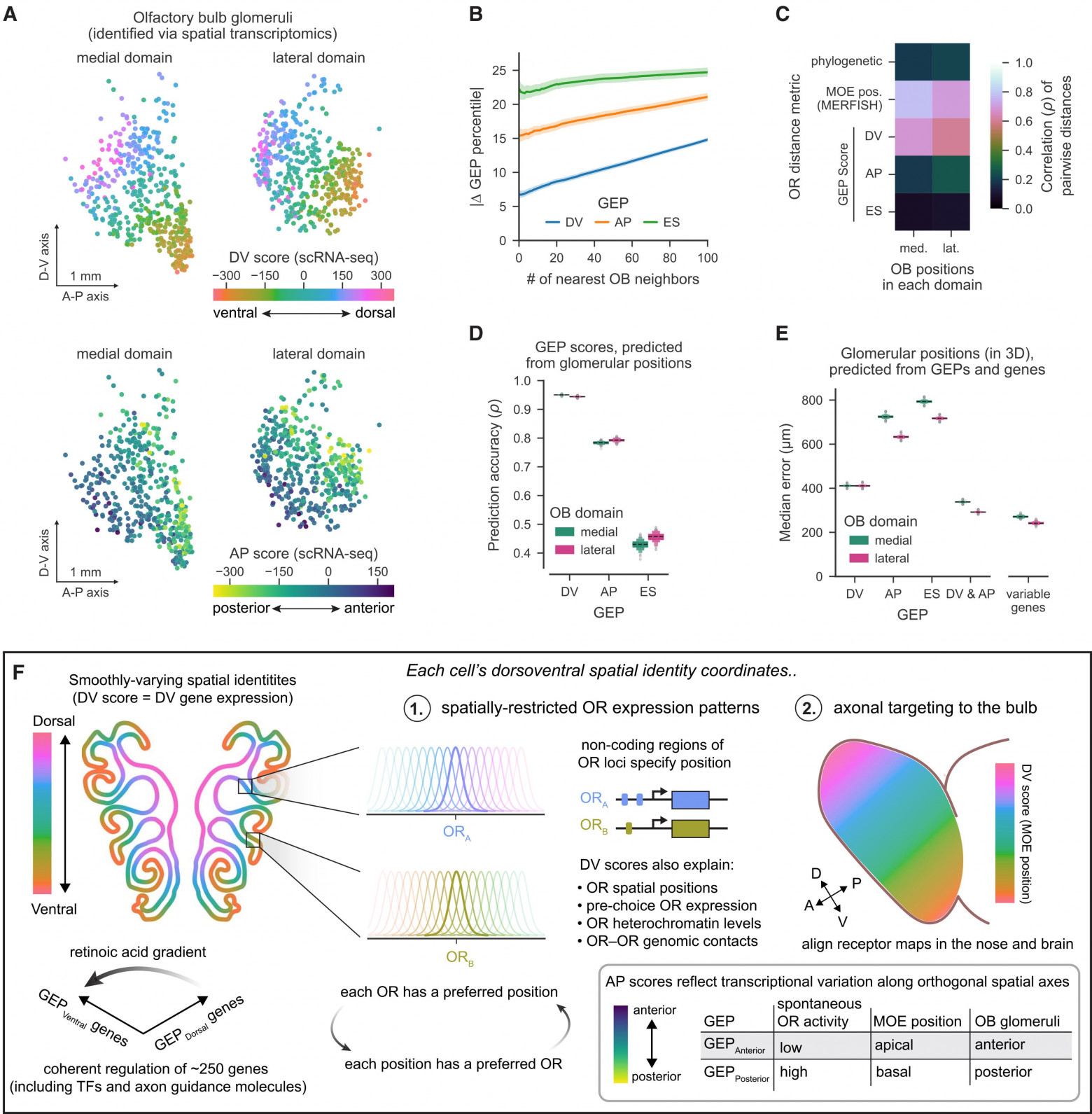
Чтобы проверить возможность того, что гены DV могут связывать пространственное положение эпителия с аксональными мишенями в обонятельной луковице, ученые воспользовались недавним набором данных пространственной транскриптомики, который идентифицировал клубочки для многих подтипов обонятельных нейронов. Окрашивание идентифицированных клубочков на основе оценок DV их соответствующих рецепторов показало, что оценки DV плавно изменяются по всей обонятельной луковице и что соседние клубочки имеют схожие оценки DV (7A–7C). В результате трехмерное положение каждого клубочка предсказывало оценку DV иннервирующего подтипа обонятельного нейрона с высокой точностью (7D), и наоборот, оценка DV каждого подтипа обонятельного нейрона предсказывала трехмерное местоположение его клубочка (медианная ошибка ≈ 400 мкм, 3–4 ширины клубочка) (7E). Таким образом, вариации в экспрессии генов DV (и, как следствие, в расположении в эпителии) у разных подтипов обонятельных нейронов могут, по крайней мере частично, объяснить пространственную организацию их аксональных проекций к луковице.
Примечательно, что AP GEP также включают гены (такие как Nrp1 и Plxna1), которые, как известно, опосредуют наведение аксонов вдоль AP-оси обонятельной луковицы, а также дополнительные гены, связанные с аксонным наведением и цитоскелетом (например, Plxna3, Sema6c, Pcdh11x, Cdh15). Аналогично DV GEP, использование AP GEP также плавно варьировалось в зависимости от клубочков обонятельной луковицы, хотя и вдоль ортогональной пространственной оси по отношению к той, которая используется DV GEP, и таким образом, что это было несколько менее предсказуемо для положения клубочка (7A–7E). Трехмерное положение клубочков для каждого подтипа обонятельных нейронов лучше всего предсказывалось путем комбинирования использования DV и AP GEP. Ошибка этих предсказаний (∼300 мкм) была аналогична той, которая наблюдалась при использовании моделей, обученных на всех ∼1300 вариабельных генах обонятельных нейронов (7E). Это указывает на то, что эти два GEP вместе эффективно суммируют соответствующие транскрипционные оси, которые отображают подтипы обонятельных нейронов на положение луковицы. Таким образом, две основные оси (DV и AP), которые организуют обонятельную луковицу, топографически и транскрипционно представлены в самом эпителии.
Для более детального ознакомления с нюансами исследования рекомендую заглянуть в доклад ученых и дополнительные материалы к нему.
Эпилог
В рассмотренном нами сегодня труде ученым удалось создать первую в мире карту обоняния, которая показывает расположение более тысячи обонятельных рецепторов внутри носа мыши.
Ранее считалось, что расположение нейронов обоняния является случайным. Однако, они на самом деле высокоорганизованы и образуют горизонтальные полосы, или отрезки, идущие от верхней части носа к нижней, сгруппированные по типу рецепторов. Ученые также показали, что эта карта в носу совпадает с соответствующими картами в обонятельной луковице головного
Понимание того, как расположены сенсорные рецепторы глаз, ушей и кожи, имеется уже довольно давно. Обоняние в этот клуб не входило довольно долго ввиду сложности. Дело в том, что у, к примеру, мышей насчитывается порядка 20 миллионов обонятельных нейронов, каждый из которых экспрессирует один из более чем тысячи типов рецепторов. В отличие от этого, цветовое зрение человека основано всего на трех основных типах рецепторов. Каждый обонятельный рецептор обнаруживает определенный набор молекул запаха, что делает систему гораздо более сложной.
В ходе исследования ученые проанализировали около 5.5 миллионов нейронов у порядка 300 особей мышей. Они объединили секвенирование отдельных клеток, которое определяет, какие рецепторы экспрессирует каждый нейрон, с пространственной транскриптомикой, которая точно определяет местоположение этих нейронов. В результате была выявлена четкая закономерность. Нейроны образуют плотно организованные, перекрывающиеся горизонтальные полосы в зависимости от рецептора, который они несут. Это расположение было практически идентичным у всех изученных животных и точно соответствовало тому, как обонятельная информация отображается в
Затем было проведено исследование того, как именно формируется обонятельная карта. Ученые определили ретиноевую кислоту, молекулу, регулирующую активность генов, как ключевой фактор. Градиент ретиноевой кислоты в носу, по-видимому, направляет нейроны, помогая каждому из них активировать правильный обонятельный рецептор в зависимости от его положения. Когда исследователи изменяли уровни этой молекулы, вся карта рецепторов смещалась вверх или вниз.
Помимо заполнения пробелов в знаниях касательно обонятельной системы, данное исследование играет крайне важную роль в поиске эффективных методов лечения потери обоняния. Чем обширнее понимание системы, тем выше вероятность исправить ее поломки.
Сейчас ученые работают над тем, чтобы понять, почему полосы рецепторов появляются в определенном порядке и существует ли такая же организация у людей. Эти знания могут помочь в разработке новых подходов, включая терапию стволовыми клетками или интерфейсы «мозг-компьютер», направленных на восстановление обоняния.
Немного рекламы
Спасибо, что остаетесь с нами. Вам нравятся наши статьи? Хотите видеть больше интересных материалов? Поддержите нас, оформив заказ или порекомендовав знакомым, облачные VPS для разработчиков от $4.99, уникальный аналог entry-level серверов, который был придуман нами для Вас: Вся правда о VPS (KVM) E5-2697 v3 (6 Cores) 10GB DDR4 480GB SSD 1Gbps от $19 или как правильно делить сервер? (доступны варианты с RAID1 и RAID10, до 24 ядер и до 40GB DDR4).
Dell R730xd в 2 раза дешевле в дата-центре Maincubes Tier IV в Амстердаме? Только у нас 2 х Intel TetraDeca-Core Xeon 2x E5-2697v3 2.6GHz 14C 64GB DDR4 4x960GB SSD 1Gbps 100 ТВ от $199 в Нидерландах! Dell R420 - 2x E5-2430 2.2Ghz 6C 128GB DDR3 2x960GB SSD 1Gbps 100TB - от $99! Читайте о том Как построить инфраструктуру корп. класса c применением серверов Dell R730xd Е5-2650 v4 стоимостью 9000 евро за копейки?
Автор: Dmytro_Kikot
