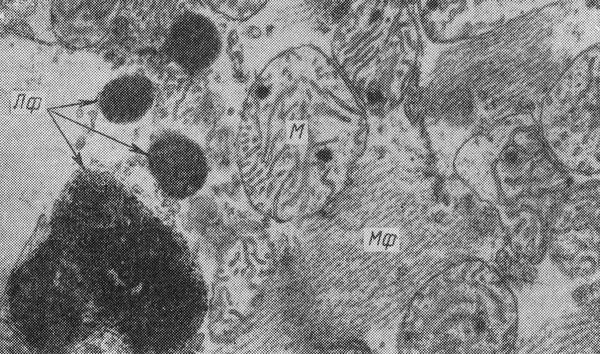Молекулярные и фенотипические биомаркеры старения.
Введение.
Для чего нужны биомаркеры старения?
Старение представляет из себя зависящий от времени физиологический функциональный спад, который поражает большинство живых организмов. И этот процесс напрямую связан с молекулярными изменениями. Он также является самым основным фактором риска для многих неинфекционных заболеваний. С одной стороны, выявление биомаркеров старения будет способствовать дифференциации людей, имеющих один и тот же хронологический возраст, но разные варианты старения. Количественные биомаркеры старения также могут составить группу измерений для «здорового старения» и, кроме этого, прогнозировать продолжительность жизни.
С другой стороны, биомаркеры старения могут также помочь исследователям сузить сферу исследований до конкретных биологических аспектов в попытках объяснить биологические процессы, связанные со старением и возрастными заболеваниями. Здесь мы рассмотрим фенотипические и молекулярные биомаркеры старения.
Фенотипические биомаркеры могут быть неинвазивными, панорамными и легкодоступными, тогда как молекулярные биомаркеры могут отражать некоторые молекулярные механизмы, лежащие в основе возрастного статуса. Этот обзор в основном рассматривает результаты, полученные в исследованиях с людьми (и в некоторых редких случаях – с лабораторными животными (мышами) и нематодами).
Молекулярные биомаркеры старения